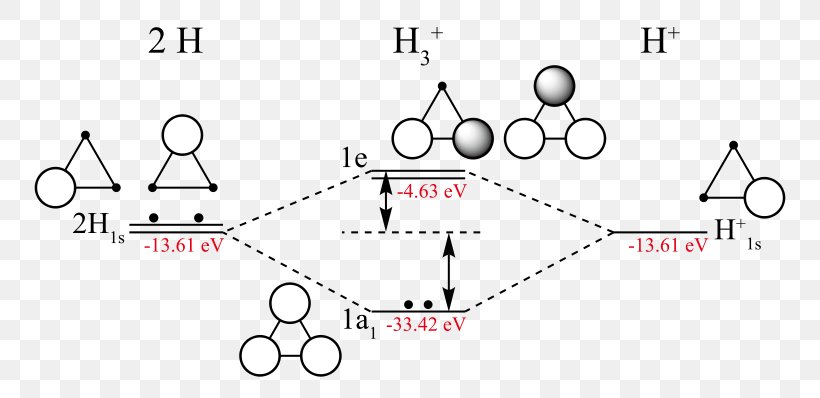
El hidrógeno triatómico, trihidrógeno o H3 es una molécula formada por tres átomos de hidrógeno, que se forma en condiciones especiales por su menor estabilidad respecto del hidrógeno molecular diatómico, H2, o del catión trihidrógeno, H3 . Pertenece al grupo de las moléculas de Rydberg,[1] moléculas predichas por Enrico Fermi y que resultan más estables en estados de alta energía que en el estado fundamental, que es disociativo. El enlace entre sus átomos es extremadamente débil y se forma porque uno de sus átomos posee un electrón muy alejado del núcleo (átomo de Rydberg) lo que le permite interactuar con los otros átomos y formar la molécula.
Descubrimiento y primeros estudios
Fue descubierta espectroscópicamente en los años 80 por Gerhard Herzberg, premio Nobel de Química en 1971 y padre de la espectroscopia molecular. Por este descubrimiento se le concedió en 1985 la medalla de la American Physical Society.[2]
Fue estudiado por el físico alemán Wolfgang Ketterle, cuya tesis doctoral versó sobre la espectroscopia del hidruro de helio y del hidrógeno triatómico, en 1986.[3]
Propiedades y reacciones
Estas moléculas se forman a presiones bajas (en torno a 2 cmHg en tubos de descarga).[4]
Tienen tendencia a autoionizarse o fotodisociarse, perdiendo un electrón para dar el catión trihidrógeno, más estable.[5]
De hecho, los estados excitados de H3 próximos al umbral de ionización son resonancias en el proceso de recombinación disociativa:[6]
y también
En la literatura
Jack Williamson escribió en 1940 un relato de ciencia ficción llamado "El paraje perdido" en el que un científico trata de convertir hidrógeno triatómico en helio-3 mediante un proceso catalítico a alta presión, para fabricar bombas atómicas.[7]
Véase también
- Dihidrógeno, H2
- Catión trihidrógeno, H3
- Catión dihidrógeno, H2
Enlaces externos
- Página sobre el hidrógeno triatómico (en inglés) del Department of Molecular and Optical Physics, Universidad de Freiburg, Alemania.
Referencias